產品型錄
產品資訊
目前顯示: 黴漿菌及耗材試劑類 / 殘留宿主細胞DNA檢測
殘留宿主細胞DNA檢測
Residual Host Cell DNA Testing
殘留宿主細胞DNA檢測是生物製藥(包括重組蛋白、單克隆抗體和基於細胞的療法)生產中品質控制的一個關鍵方面。宿主細胞 DNA 是指源自用於生產生物製藥產品的細胞系的遺傳物質。為此,經常使用 CHO、HEK-293 和大腸桿菌細胞。即使經過廣泛的下游純化過程,最終產品中仍可能殘留微量的宿主細胞 DNA,從而帶來潛在的安全和監管問題。
WHO、FDA 和歐洲藥典建議最終產品中的殘留DNA濃度低於10 ng/劑量。
Minerva Biolabs 開發了一種dPCR 檢測方法,用於檢測大腸桿菌、CHO 或 HEK-293 的殘留宿主細胞 DNA - MiQuant® Residual DNA HEK-293 – dPCR。使用 dPCR 可縮短獲得結果的時間,因為在 dPCR 分析之前不需要樣品製備,並且無需標準曲線即可進行絕對定量。在 dPCR 驗證標準品的説明下,可以確定基質特異性轉換因數,該因數將 [copies/µl] 轉化為 [fg/μl],以提供符合監管指南的殘留 DNA 的定量。
dPCR Validation Standard HEK-293
58-0221: HEK-293
ldPCR 驗證標準 HEK-293 可用於通過連續稀釋生成 HEK-293 細胞系的標準曲線。通過該標準曲線,測得的DNAcopies/µl可轉換為 fg/μl,從而根據監管指南對殘留 DNA 進行定量。此外,dPCR 驗證標準品可用於下游流程,以檢查不同純化過程中處理樣品的殘留DNA濃度。
MiQuant® Residual DNA HEK-293 – dPCR
58-0121 : 35 µl primer/probe mix
58-0122 : 140 µl primer/probe mix
l足以擴增高度降解的 HEK-293 DNA
l新穎、快速、穩定和靈敏的方法
l快速的工作流程,因為 dPCR 分析前不需要樣品製備
l符合 EP、WHO 和 FDA 標準
l相容 QIAcuity®、ddPCR™、Quantstudio™ Absolute Q™
l凍幹試劑,簡化了物流和儲存
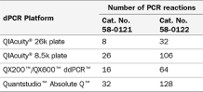
由於每個 dPCR 設備需要不同的 PCR 反應體積,因此 PCR 反應次數如表所示。

 繁體中文
繁體中文  English
English